一、分类管理:
中国对医疗器械产品按照风险程序将其分为三类(即I类、II类和III类医疗器械),实行分类管理,不同类别的医疗器械产品,其注册、备案、许可程序及要求也不一样, 因此在医疗器械注册及相关许可申请之前确定产品分类是非常关键的。
一类医疗器械:风险程度低,实行常规管理可以保证其安全、有效的医疗器械。
二类医疗器械:具有中度风险,需要严格控制管理以保证其安全、有效的医疗器械。
三类医疗器械:具有较高风险,需要采取特别措施严格控制管理以保证其安全、有效的医疗器械。
医疗器械分类的确定需要考虑产品的预期用途、结构特征和使用方法,并依据医疗器械分类规则、分类目录及现有产品标准等进行判定,必要时也可以申请分类界定申请,食品药品监督管理部门将组织专家对提交申请的产品进行分析并归类。
二、申请条件:
①企业的生产、质量和技术负责人应当具有与所生产医疗器械相适应的专业能力,并掌握国家有关医疗器械监督管理的法律、法规和规章以及相关产品质量、技术的规定。质量负责人不得同时兼任生产负责人;
②企业内初级以上职称或者中专以上学历的技术人员占职工总数的比例应当与所生产产品的要求相适应;
③企业应当具有与所生产产品及生产规模相适应的生产设备,生产、仓储场地和环境。企业生产对环境和设备等有特殊要求的医疗器械的,应当符合国家标准、行业标准和国家有关规定;
④企业应当设立质量检验机构,并具备与所生产品种和生产规模相适应的质量检验能力;
⑤企业应当保存与医疗器械生产和经营有关的法律、法规、规章和有关技术标准;
⑥开办医疗器械生产企业应当符合国家医疗器械行业发展规划和产业政策。
三、所需资料
1《医疗器械生产企业许可证》(开办)申请表;
2法定代表人、企业负责人的基本情况及资质证明,包括身份证明,学历证明,职称证明,任命文件的复印件,工作简历;
3工商行政管理部门出具的企业名称核准通知书或营业执照原件和复印件;
4生产场地证明文件,包括房产证明或租赁协议和被租赁方的房产证明的复印件,厂区总平面图,主要生产车间布置图。有洁净要求的车间,须标明功能间及人物流走向;
5企业的生产、技术、质量部门负责人简历,学历和职称证书的复印件;相关专业技术人员、技术工人登记表、证书复印件,并标明所在部门及岗位;高、中、初级技术人员的比例情况表;内审员证书复印件;
6拟生产产品范围、品种和相关产品简介。产品简介至少包括对产品的结构组成、原理、预期用途的说明及产品标准;
7主要生产设备及检验仪器清单;
8生产质量管理规范文件目录:
9拟生产产品的工艺流程图,并注明主要控制项目和控制点。包括关键和特殊工序的设备、人员及工艺参数控制的说明;
10拟生产无菌医疗器械的,需提供洁净室的合格检测报告。由省级食品药品监督管理部门认可的检测机构出具的一年内的符合《无菌医疗器具生产管理规范》(YY0033-2000)的合格检验报告;
11申请材料真实性的自我保证声明。列出申报材料目录,并对材料作出如有虚假承担法律责任的承诺。
四、服务流程
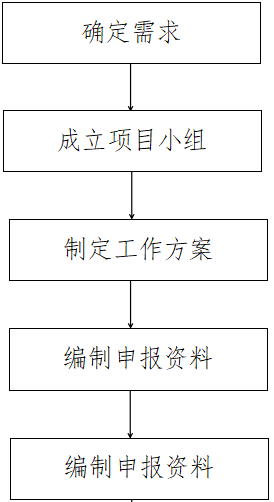
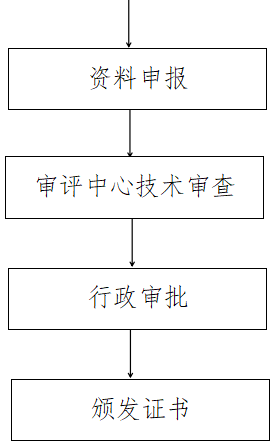
五、服务内容
1. 提供确认生产场地符合要求的相关咨询服务
2. 提供确认生产、检验设备符合要求的相关咨询服务
3. 提供人员团队建立的咨询服务
4. 提供产品试生产相关技术咨询服务
5. 提供试生产过程风险评估及管理的服务
6. 提供批生产记录制作的咨询服务
7. 提供产品相关工艺验证的咨询服务
8. 提供质量管理体系文件咨询服务