1. 医疗器械注册
医疗器械注册是食品药品监督管理部门根据医疗器械注册申请人的申请,依照法定程序,对其拟上市医疗器械的安全性、有效性研究及其结果进行系统评价,以决定是否同意其申请的过程。
2. 服务内容
分类界定:帮助企业对拟申报注册产品进行分类查询。查询《分类目录》或“分类界定的通知”文件,确定拟申报注册产品的分类依据。若《分类目录》或“分类界定的通知”文件没有改产品的分类依据,则需按照《医疗器械分类规则》进行分类判定,并在分类界定系统中进行申请,同时提交纸质资料至省食品药品监督管理局。
注册检验:帮助企业编制产品技术要求、说明书等资料,协助联系具有医疗器械检验资质检验机构进行检验,跟踪检验进度、协助解决检验过程中出现的问题。
临床试验:帮助企业查询临床豁免目录以及同类产品信息,确定拟注册产品是否可以豁免临床,如不能豁免,则协助企业进行临床试验。
产品注册:编制产品注册资料并协助进行注册申报,帮助企业解决在技术评审过程中遇到的整改问题。
体系核查:帮助企业建立医疗器械质量管理体系,包含质量手册、程序文件、管理制度、作业文件、记录表单。指导企业运行管理体系,并保持质量记录;指导企业对生产设备、工艺过程进行验证;指导企业进行内审和管理评审;指导企业对生产车间、仓库进行布置;对企业质量管理运行过程和结果进行审核;指导企业迎接药品监督管理部门的现场体系核查。
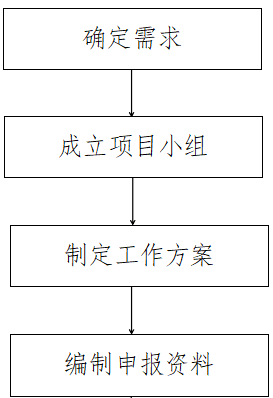
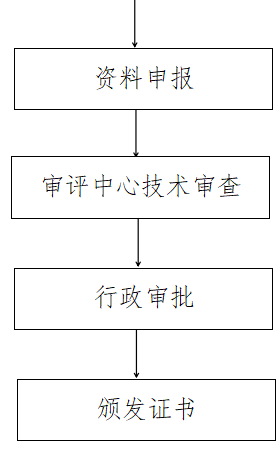
3.服务流程